Bioingeniería
Primer trasplante en cerdos de riñones porcinos modificados con organoides renales humanos
Unos científicos han desarrollado una tecnología pionera que permite producir organoides renales humanos de manera ampliable, combinarlos con riñones de cerdo fuera del cuerpo y trasplantarlos de nuevo al mismo animal de manera viable.
Este avance es obra de un equipo liderado por el Instituto de Bioingeniería de Cataluña (IBEC), en colaboración con el Instituto de Investigación Biomédica de A Coruña (INIBIC), en España, y grupos de investigación internacionales.
Lo logrado representa un hito en el campo de la medicina regenerativa y personalizada, estableciendo las bases para la utilización de organoides de riñón derivados de células madre humanas para terapia celular en ensayos clínicos.
Este trabajo, liderado por la Dra. Núria Montserrat, investigadora principal en el IBEC en el momento del estudio, es el resultado de una trayectoria científica de más de una década dedicada a la medicina regenerativa y a la bioingeniería de órganos. Fruto de esta línea de investigación sostenida, el equipo de investigación ha conseguido combinar por primera vez organoides renales humanos con riñones porcinos vivos, conectados a máquinas de perfusión normotérmica. El uso de estos dispositivos, utilizados habitualmente en el quirófano para mantener el órgano vivo y oxigenado fuera del cuerpo antes de un trasplante, ha permitido insertar organoides humanos dentro de los riñones porcinos y monitorear en tiempo real su integración y función.
"Nuestra investigación demuestra que la combinación de tecnologías de organoides y perfusión ex vivo puede permitir intervenciones celulares en condiciones totalmente controladas." explica la Dra. Montserrat. "El objetivo a largo plazo es poder regenerar o reparar un órgano antes del trasplante. Esto podría reducir el tiempo de espera de los pacientes crónicos y aumentar el número de órganos viables para el trasplante."
Un organoide de riñón es una estructura tridimensional, de unas micras de tamaño, cultivada en el laboratorio a partir de células madre humanas. Aunque no es un órgano completo, reproduce muchas de sus estructuras y funciones principales. Gracias a estas características, los organoides permiten estudiar cómo se desarrolla el riñón, probar nuevos fármacos y, en el futuro, se espera que puedan ser utilizados para reparar tejidos renales dañados o mejorar órganos destinados al trasplante.
El nuevo método es capaz de producir miles de estos organoides renales humanos, utilizando técnicas de microagregación e ingeniería genética.
![[Img #77266]](https://noticiasdelaciencia.com/upload/images/11_2025/7081_primer-trasplante-en-cerdos-de-rinones.jpg)
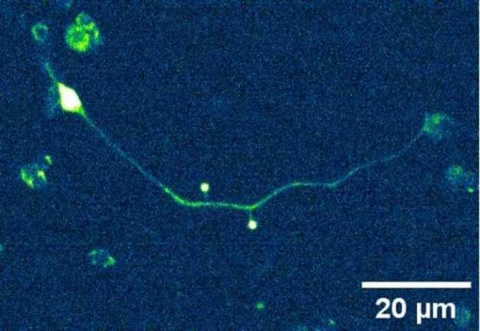
Imagen de un organoide de riñón en el día 16 de diferenciación obtenida por microscopía confocal. Las células han sido marcadas con diferentes colores mediante la técnica de inmunofluorescencia para identificar componentes específicos: LTL (verde: túbulos renales), WT1 (rojo: podocitos), PODXL (amarillo: podocitos) y DAPI (azul: núcleos celulares). Esta imagen permite observar cómo se organizan los diferentes tipos de células dentro del organoide renal. (Imagen: IBEC)
"A pesar del gran potencial clínico de los organoides, hasta ahora uno de los grandes retos para aplicar esta tecnología en tratamientos médicos reales era conseguir producir estos organoides de manera escalable, uniforme y asequible. Ahora, con nuestro nuevo método, podemos generar miles de organoides renales en condiciones controladas y en poco tiempo, con una gran precisión y sin necesidad de componentes complejos", añade la Dra. Elena Garreta, investigadora del grupo de Puripotencia para la regeneración de órganos del IBEC y coprimera autora del estudio.
Por otro lado, la utilización de las máquinas mencionadas, para llevar a cabo la perfusión de los organoides dentro de los riñones, ofrece una ventaja clave: permite medir parámetros fisiológicos del órgano en tiempo real y detectar de manera inmediata cualquier signo de daño o rechazo. Los experimentos se realizaron tanto ex vivo (fuera del organismo) como in vivo (en el mismo animal), utilizando un modelo porcino de trasplante muy similar al riñón humano.
El equipo observó que, después de 24 y 48 horas del trasplante, los organoides humanos persistían integrados en el tejido renal porcino, mantenían su viabilidad y no desencadenaban ninguna respuesta inmune significativa. El riñón trasplantado continuaba funcionando con normalidad, y no se detectaron signos de daño ni toxicidad.
Esta metodología permite imaginar un escenario clínico en el que los órganos destinados al trasplante puedan ser tratados y acondicionados antes de implantarlos. En este contexto, la colaboración con el Instituto de Investigación Biomédica de A Coruña (INIBIC), la Organización Nacional de Trasplantes (ONT) y otras instituciones, como el Instituto de Salud Carlos III (ISCIII), en España, ha sido esencial para trasladar la investigación a un entorno quirúrgico realista y preclínico.
El equipo de investigación expone los detalles técnicos del nuevo método en la revista académica “Nature Biomedical Engineering”, bajo el título “Systematic production of human kidney organoids for transplantation in porcine kidneys during ex vivo machine perfusion”. (Fuente: IBEC)